冠状病毒样颗粒COVID-19候选疫苗(CoVLP)是一款植物源性重组COVID-19疫苗,由表达为病毒样颗粒(VLPs)的重组刺突(S)糖蛋白及佐剂 (Adjuvant System 03 [AS03])组成。在早期的研究中,CoVLP+AS03 疫苗(Covifenz,Medicago)诱导了强大而持久的中和抗体水平和平衡的 T 细胞反应(干扰素-γ 和白细胞介素 4),这两者都可能有助于保护。
2022年5月4日,加拿大Medicago公司的Brian J. Ward团队在国际知名期刊新英格兰医学杂志NEJM(IF=91)在线发表题为“Efficacy and Safety of a Recombinant Plant-Based Adjuvanted Covid-19 Vaccine”的研究论文,该研究在 85 个中心进行的多国、随机、安慰剂对照试验中,以 1:1 的比例分配成年人(≥18 岁)接受两次肌肉注射 CoVLP+AS03 疫苗或安慰剂,间隔 21 天。该试验的主要目的是确定 CoVLP+AS03 疫苗在第二次注射后至少 7 天开始预防症状性冠状病毒病 2019 (Covid-19) 的功效,并在检测到至少 160 例病例后进行分析。
共有24141名志愿者参加了试验;参与者的中位年龄为29岁。针对由测序鉴定的五种变异引起的任何症状性 Covid-19,疫苗的有效性为 69.5%(95% 置信区间 [CI],56.7 至 78.8)。在一项事后分析中,疫苗对中度至重度疾病的有效性为 78.8%(95% CI,55.8 至 90.8),在基线时血清阴性的参与者中为 74.0%(95% CI,62.1 至 82.5)。疫苗组未发生严重的 Covid-19 病例,其中突破病例的中位病毒载量比安慰剂组低 100 倍以上。引起的不良事件大多是轻度或中度和短暂的,并且是疫苗组比安慰剂组更频繁;局部不良事件发生率分别为 92.3% 和 45.5%,全身性不良事件发生率分别为 87.3% 和 65.0%。两组在每次给药后长达 21 天(22.7% 和 20.4%)以及从第 43 天到第 201 天(4.2% 和 4.0%)的主动不良事件发生率相似。总之,该研究发现CoVLP+AS03 疫苗可有效预防由一系列变异引起的 Covid-19,其功效范围从针对症状感染的 69.5% 到针对中重度疾病的 78.8%。
最后,2022年2月24日,Medicago和葛兰素史克(GSK)宣布,加拿大卫生部批准了其生产的新型冠状病毒疫苗,商品名COVIFENZ?。该疫苗是世界首个获批的植物源人体疫苗。加拿大已成为全球第一个授权使用基于植物新冠疫苗的国家。加拿大监管机构表示,允许Medicago公司的两剂新冠疫苗为18至64岁的成年人接种,但表示65岁及以上人群的相关数据还太少。

自 2019 年以来,SARS-CoV-2已导致超过 4.97 亿例Covid-19病例,并导致全球 610 万人死亡。刺突 (S) 糖蛋白是大多数这些疫苗中的抗原,而 S 特异性中和抗体与预防感染有关。尽管与平台相关的不良事件很少发生,但几种疫苗已成功部署并且具有可接受的安全性。
最近,据报道,由于免疫力下降和变异体的出现导致保护作用降低。正在部署加强针以恢复中和抗体水平并改善对一系列变异体的交叉保护。高水平疫苗接种人群对加强针的需求和未接种人群对初始疫苗接种的需求造成的紧张局势表明,需要额外的疫苗来满足全球需求。
一种冠状病毒样颗粒 (CoVLP) 疫苗正在基于植物的平台上生产,该平台已被用于生产多种病毒疫苗,这些疫苗已显示出显著的免疫原性和功效。在植物叶子的细胞中, SARS-CoV-2 S 蛋白的表达导致形成 100 至 150 nm 的病毒样颗粒(Medicago是利用一种烟草植物的病毒样颗粒,其蛋白有类似新冠病毒的外壳,但缺少病毒的基因组,因此完全无害。它模拟新冠病毒的外部结构,令它们很容易被免疫系统识别)。收获和纯化后,这些颗粒在 2 至 8°C 下可稳定至少 6 个月。
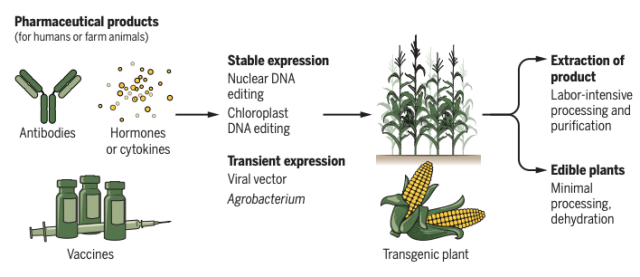
植物生产疫苗的过程(图源自Science )
Adjuvant System 03 (AS03, GlaxoSmithKline) 启动短暂的先天反应并增加适应性反应的幅度、质量和持久性。AS03 已用于大流行性流感疫苗以及其他许可和候选疫苗。在早期的研究中,CoVLP+AS03 疫苗(Covifenz,Medicago)诱导了强大而持久的中和抗体水平和平衡的 T 细胞反应(干扰素-γ 和白细胞介素 4),这两者都可能有助于保护。在这里,该研究报告了 CoVLP+AS03 疫苗关键 3 期试验的早期结果,以评估其有效性和安全性。
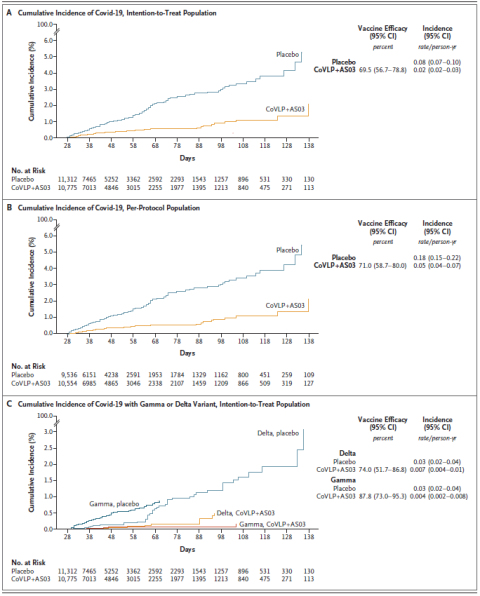
根据人口和变异的存在,Covid-19 的累积发病率(图源自NEJM )
该研究在 85 个中心进行的多国、随机、安慰剂对照试验中,以 1:1 的比例分配成年人(≥18 岁)接受两次肌肉注射 CoVLP+AS03 疫苗或安慰剂,间隔 21 天。该试验的主要目的是确定 CoVLP+AS03 疫苗在第二次注射后至少 7 天开始预防症状性冠状病毒病 2019 (Covid-19) 的功效,并在检测到至少 160 例病例后进行分析。
共有24141名志愿者参加了试验;参与者的中位年龄为29岁。针对由测序鉴定的五种变异引起的任何症状性 Covid-19,疫苗的有效性为 69.5%(95% 置信区间 [CI],56.7 至 78.8)。在一项事后分析中,疫苗对中度至重度疾病的有效性为 78.8%(95% CI,55.8 至 90.8),在基线时血清阴性的参与者中为 74.0%(95% CI,62.1 至 82.5)。疫苗组未发生严重的 Covid-19 病例,其中突破病例的中位病毒载量比安慰剂组低 100 倍以上。
引起的不良事件大多是轻度或中度和短暂的,并且是疫苗组比安慰剂组更频繁;局部不良事件发生率分别为 92.3% 和 45.5%,全身性不良事件发生率分别为 87.3% 和 65.0%。两组在每次给药后长达 21 天(22.7% 和 20.4%)以及从第 43 天到第 201 天(4.2% 和 4.0%)的主动不良事件发生率相似。总之,该研究发现CoVLP+AS03 疫苗可有效预防由一系列变异引起的 Covid-19,其功效范围从针对症状感染的 69.5% 到针对中重度疾病的 78.8%。
最后,2022年2月24日,Medicago和葛兰素史克(GSK)宣布,加拿大卫生部批准了其生产的新型冠状病毒疫苗,商品名COVIFENZ?。该疫苗是世界首个获批的植物源人体疫苗。加拿大已成为全球第一个授权使用基于植物新冠疫苗的国家。加拿大监管机构表示,允许Medicago公司的两剂新冠疫苗为18至64岁的成年人接种,但表示65岁及以上人群的相关数据还太少。
(来源:iNature)
原文出处:Hager KJ, Pérez Marc G, Gobeil P, et al. Efficacy and Safety of a Recombinant Plant-Based Adjuvanted Covid-19 Vaccine. N Engl J Med. 2022 May 4. doi: 10.1056/NEJMoa2201300. Epub ahead of print. PMID: 35507508.
链接:https://pubmed.ncbi.nlm.nih.gov/35507508/